Уксусная кислота вода. Области применения уксусной кислоты
Название:
Уксусная кислота (этановая кислота)- одноосновная карбоновая кислота алифатического ряда.
Химическая формула:
История открытия:
Уксусная кислота известна с древнейших времен, так как образуется при скисании вин (винный уксус).
Но строением уксусной кислоты и причиной возникновения, ученые заинтересовались лишь после сенсационного опубликования Дюма эмпирического правила замещения в органических соединениях водорода хлором. До этого в химии господствовала теория, выдвинутая Йенсом Якобом Берцелиусом. Он распределил элементы на электроположительные и электроотрицательные, и полностью отрицал замещения водорода и хлора соответственно, без изменения химического строения веществ.
В своей работе 1839 года Дюма для шведской академии представил отчет, в котором освятил начальные принципы, сформулированного им эмпирического правила для органических веществ, и для уксусной кислоты в частности: “В неорганической химии путеводной нитью нам служит изоморфизм, теория, основанная на фактах, как хорошо известно, мало согласных с электрохимическими теориями. В органической химии ту же роль играет теория замещения... и может быть будущее покажет, что оба воззрения более тесно связаны между собою, что они вытекают из одних и тех же причин и могут быть обобщены под одним и тем же названием.”
К такому заключению он шел несколько лет. Свои первые опыты Дюма начал с исследования уксусной кислоты, и превращения ее в хлоруксусную. Водород в этой реакции полностью замещается хлором, в соотношении 1:1, и самое главное без утраты основных химических свойств и отношения вещества к классу. Дальнейшие опыты с замещением водорода йодом и бромом окончательно убедили ученого в этом.
Революционным оказался вывод о принципиальном различии образования неорганических и органических соединений.
Однако, Берцелиус, защищая свою теорию, приводит пример щавелевой кислоты, и полученной соли при соединении ее с хлоридом, а значит утрате кислотных свойств. Он утверждает на примере как органических, так и неорганических соединениях что их кислородсодержащая часть может вступать в реакцию с основаниями и их лишаться, не теряя связи с хлорсодержащей частью. Именно этот аспект, по мнению химика, основное упущение, сделанное Дюма в своих опытах, т.к. он не опровергнул и не подтвердил этого известного факта.
Чтобы как-то объяснить, полученные Дюма результаты, Берцелиус выдвигает предположение: “хлоруксусная кислота Дюма,
очевидно, принадлежит к этому классу соединений; в ней радикал углерода соединен
и с кислородом, и с хлором. Она может быть, следовательно, щавелевой кислотою, в
которой половина кислорода замещена хлором, или же соединением 1 атома
(молекулы) щавелевой кислоты с 1 атомом (молекулой) полуторохлористого углерода
C2Cl6. Первое предположение не может быть принято, потому что оно допускает
возможность замещения хлором 11/2, атомов кислорода (По Берцелиусу щавелевая
кислота была C2O3.). Дюма же держится третьего представления, совершенно
несовместимого с двумя вышеизложенными, по которому хлор замещает не кислород, а
электроположительный водород, образуя углеводород C4Cl6, обладающий теми же
свойствами сложного радикала, как и C4H6 или ацетил, и способный якобы с 3
атомами кислорода давать кислоту, тожественную по свойствам с У., но, как видно
из сравнения (их физических свойств), вполне от нее отличную"
Но семена, заложенные Дюма, давали свои всходы. Теперь многие ученные отвернувшись от теории Берцелиуса продолжали нововведения. Так Шарль Фредерик Жерар впервые вопреки теории радикалов (создателем и приверженцем которой был Берцелиус) установил, что радикалы не существуют самостоятельно, а представляют собой атомные группы – “остатки”, комбинация которых образует молекулу. В своем очерке “Об основности кислот” в 1851 году он развил теорию типов, согласно которой все химические соединения можно классифицировать как производные четырех типов – водорода, хлороводорода, воды и аммиака. В частности была мысль об сходности конституции трихлоруксусной кислоты и уксусной кислоты. В свою защиту Берцелиус парирует: “Жерар высказал новый взгляд на состав спирта, эфира и их
производных; он следующий: известное соединение хрома, кислорода и хлора имеет
формулу = CrO2Cl2, хлор замещает в нем атом кислорода (Подразумевается
Берцелиусом 1 атом кислорода хромового ангидрида - CrO3). У. кислота C4H6+3O
заключает в себе 2 атома (молекулы) щавелевой кислоты, из которых в одном весь
кислород замещен водородом = C2O3+C2H6.” Но такая игра цифрами не удержала авторитета теории и год спустя Дюма наносит сокрушительный удар, развив теорию типов, исследуя сходные свойства трихлоруксусной кислоты и уксусной кислоты в реакции разложения, под влиянием щелочей.
С другой стороны, Либих и Греэм публично высказались за
большую простоту, достигаемую на почве теории замещения, при рассмотрении
хлоропроизводных обыкновенного эфира и эфиров муравьиной и У. кисл., полученных
Малагутти.
Берцелиус, уступая давлению новых фактов, в 5-м изд. своего
"Lehrbuch der Chemie" (Предисловие помечено ноябрем 1842 г.) , на стр. 709,
позабыв свой резкий отзыв о Жераре, нашел возможным написать следующее: "Если мы
припомним превращение (в тексте разложение) У. кислоты под влиянием хлора в
хлорощавелевую кислоту (Хлорощавелевой - Chloroxalsaure - Берцелиус называет
трихлоруксусную кисл. , то представляется
возможным еще другой взгляд на состав У. кислоты, а именно - она может быть сочетанной щавелевой кислотой, в которой сочетающейся группой (Paarling) является C2H6, подобно тому, как сочетающейся группой в хлорощавелевой кислоте является C2Cl6, и тогда действие хлора на У. кислоту состояло бы только в превращении C2H6 в C2Cl6. Понятно, нельзя решить, является ли такое представление более правильным..., однако, полезно обратить внимание на возможность его".
Но в полку сторонников теории типов все прибывало. Исходной точкой для работ Кольбе послужило изучение кристаллического вещества, состава CCl4SO2, полученного ранее Берцелиусом и Марсэ при действии царской водки на CS2 и образовавшегося у Кольбе при действии на CS2 влажного хлора. Рядом превращений Кольбе показал, что это
тело представляет, выражаясь современным языком, хлор ангидрид
трихлорометилсульфоновой кислоты, CCl4SO2 = CCl3.SO2Cl способный под влиянием щелочей давать соли соответственной кислоты - CCl3.SO2(OH), которая под влиянием цинка замещает сначала один атом Сl водородом, образуя кислоту CHCl2.SO2(OH) Гидратная вода, по обыкновению, Берцелиусом не принимается
во внимание.), а затем и другой, образуя кислоту CH2Cl.SO2(OH) [по Кольбе -
Chlorelaylunterschwefelsaure], а, наконец, при восстановлении током или калиевой
амальгамой (Реакция незадолго перед тем была применена Мельсансом для
восстановления трихлоруксусной кислоты в уксусную.) замещает водородом и все три
атома Сl, образуя метилсульфоновую кисл. CH3.SO2(OH) [по Кольбе -
Methylunterschwefelsaure].
Аналогия этих соединений с хлороуксусными кислотами
невольно бросалась в глаза; действительно, при тогдашних формулах получались два
параллельных ряда, как видно из следующей таблички: H2O+C2Cl6.S2O5
H2O+C2Cl6.C2O3 H2O+C2H2Cl4.S2O5 H2O+C2H2Cl4.C2O3 H2O+C2H4Cl2.S2O5
H2O+C2H4Cl2.C2O3 H2O+C2H6.S2O5 H2O+C2H6.C2O3 Это и не ускользнуло от Кольбе,
который замечает (I. с. стр. 181): "к описанным выше сочетанным сернистым
кислотам и непосредственно в хлороуглеродсернистой кислоте (выше -
H2O+C2Cl6.S2O5) примыкает хлорощавелевая кислота, известная еще под названием
хлоруксусной кислоты. Жидкий хлороуглерод - ССl (Сl=71, С=12; теперь мы пишем
C2Cl4 - это хлороэтилен.), как известно, превращается на свету под влиянием
хлора в - гексахлорэтан и можно ожидать, что, если бы его одновременно подвергнуть действию воды, то он, подобно хлористому висмуту, хлорной сурьме и т. д., в момент образования, заместит хлор кислородом. Опыт подтвердил предположение". При действии света и
хлора на C2Cl4, находившийся под водою, Кольбе получил на ряду с гексахлорэтаном
и трихлоруксусную кислоту и выразил превращение таким уравнением: (Так как С2Сl4
может быть получен из CCl4 при пропускании его через накаленную) трубку, а ССl4
образуется при действии, при нагревании, Cl2 на CS2 то реакция Кольбе была
первым по времени синтезом У. кислоты из элементов.) "Образуется ли одновременно
и свободная щавелевая кисл., трудно решить, так как на свету хлор тотчас же
окисляет ее в У. кислоту"...
Воззрение Берцелиуса на хлоруксусную кислоту
"удивительным образом (auf eine tiberraschende Weise) подтверждается
существованием и параллелизмом свойств сочетанных сернистых кислот, и, как мне
кажется (говорит Кольбе I. с. стр. 186), выходит из области гипотез и
приобретает высокую степень вероятности.
Его предвидение о дальнейших открытиях природы органических кислот подтверждается статьей, в которой он, опираясь на опыты пишет: “Не
невероятно, что мы будем принуждены в будущем принять за сочетанные кислоты
значительное число тех органических кислот, в которых в настоящее время, в силу
ограниченности наших сведений - мы принимаем гипотетическиe радикалы...".
Ему же свойственна теория радикалов, подтверждая уже ранее высказанное он также добавляет: "Что касается явлений замещения в этих сочетанных кисл., то они получают простое объяснение в том обстоятельстве, что различные, вероятно, изоморфные соединения способны замещать друг друга в роли сочетающихся групп не изменяя существенно кислых свойств сочетанного с ними тела!"
Дальнейшее экспериментальное подтверждение этого взгляда мы находим в статье Франкланда и Кольбе: “Исходя из представления, что все кислоты ряда
(CH2)2nO4, построены подобно метилщавелевой кислоте (Теперь мы пишем CnH2nO2 и
называем метилщавелевую кислоту – уксусной. Сочетанный в
муравьиной кислоте водород участвует в реакции только тем, что он, соединяясь с
цианом, образует синильную кислоту: Обратное образование муравьиной кислоты из
синильной под влиянием щелочей представляет не что иное, как повторение
известного превращения растворенного в воде циана в щавелевую кислоту и аммиак,
с тою лишь разницей; что в момент образования щавелевая кислота сочетается с
водородом синильной кислота ".
То, что цианистый бензол (С6H5CN), напр., по Фелингу, не обладает кислыми свойствами и не образует берлинской лазури может быть, по мнению Кольбе и Фанкланда, поставлено в параллель с неспособностью хлора хлористого этила к реакции с AgNO3, и правильность их наведения Кольбе и
Франкланд доказывают синтезом по методу нитрилов (Нитрилы ими получались
перегонкой серновинных кислот с KCN (методом Дюма и Малагутти с Лебланом):
R".SO3(OH)+KCN=R.CN+KHSO4) У., пропионовой (по тогдашнему, мет-ацетоновой,) и
капроновой кислоты.
Затем, в следующем году Кольбе подверг электролизу щелочные
соли одноосновных предельных кислот и, в согласии со своей схемой, наблюдал при
этом, при электролизе Уксусной кислоты, образование этана, угольной кислоты и
водорода:
H2O+C2H6.C2O3=H2+,
а при электролизе валериановой - октана, угольной же кислоты и водорода: H2O+C8H18.C2O3=H2+ .
Работами Кольбе строение уксусной кислоты, а вместе с тем и всех
других органических кислот было окончательно выяснено и роль последующих химиков
свелась только к делению - в силу теоретических соображений и авторитета Жерара,
формул Кольбе пополам и к переведению их на язык структурных воззрений,
благодаря чему формула C2H6.C2O4H2 превратилась в CH3.CO(OH).
Способы получения:
Основной технический метод получения уксусной кислоты – окисление ацетальдегида кислородом воздуха в присутствии марганцевых катализаторов.
ацетальдегид уксусная кислота
Химические свойства:
Взаимодействие с:
Металлами
Уксусная к-та Ацетат магния
Применение:
Уксусная кислота широко используется в промышленности для:
- Консервирования мясных и рыбных продуктов,
- Изготовления синтетического (ацетатного) волокна,
- Производства гербицидов,
- Синтеза душистых веществ и растворителей,
- В кожевенной, текстильной и других отраслях промышленности,
- Широко используется соли уксусной кислоты – ацетаты.
Бесспорно, самым универсальным из известных растворителей, относящихся к алифатическим одноосновным кислотам, является всем известная уксусная кислота. Она имеет также и другие названия: уксусная эссенция или этановая кислота. Дешевизна и доступность в разных концентрациях (от 3 до 100%) данного вещества, его устойчивость и простота очистки, привели к тому, что на сегодня это лучшее и самое известное средство, обладающее свойствами растворять большинство веществ органического происхождения, пользующееся огромным спросом в различных сферах человеческой деятельности.
Уксусная кислота и, соответственно, возможности ее применения в отдельных производствах, может различаться по степени концентрации. Делиться она на пищевую, то есть уксус (3-15%), и техническую – уксусную эссенцию (70-80%) и ледяную (100%).
Как на бытовом уровне, так и, в общем, в пищевой промышленности, пользуется немалым спросом низко концентрированный раствор, процент уксусной кислоты в котором составляет около 3-15%. Им приправляют готовые блюда, используют для ароматизатизации ряда продуктов, он незаменим при консервировании, мариновании, а также солении продукции из мяса и рыбы и т.п.
Техническая уксусная кислота 70, купить которую, в отличие от пищевой, нельзя в обычном продуктовом магазине, активно применятся в химической промышленности, как прекрасное растворяющее средство, и химический реактив, синтезирующий другие вещества, к примеру, ацетон.
Техническая уксусная эссенция часто используется в медицинской (например, аспирин), целлюлозно-бумажной (в крашении и книгопечатании), лакокрасочной, текстильной парфюмерной, кожевенной и других промышленных областях. Ее используют для соединения душистых веществ, производства гербицидов, создания ацетатного (синтетического) волокна.
Значимость уксусной кислоты в медицинской и фармацевтической промышленности также велика. Это вещество является неотъемлемой составляющей ряда медикаментов и лекарственных средств, таких как уксуснокислые соли свинца и алюминия, ацетилсалициловая кислота. В комплексе их используют при лечении многочисленных воспалительных процессов и разных заболеваний, в основном педикулеза, алкогольного отравления, лишаев, радикулитов, полиартритов и т.п.
Уксусную эссенцию, также как и растворитель 646, цена на который тоже невелика, можно купить практически в любом без исключения магазине хозяйственных товаров. Также достаточно быстро заказать и купить ее можно через интернет. По стоимости обойдется дешевле. Особенно это выгодно тем, кто работает в промышленности, где требуются немалые объемы и где уксусная кислота, как и другие химические растворители , реализуется во много литражных бутылях и бочках. Поэтому покупать ее лучше всего у уже поставщиков, которые успели прекрасно зарекомендовать себя и свой товар на данном рынке.
Просмотрено: 11,857 раз
Уксусная кислота (Acetic acid, этановая кислота, E260) — слабая, предельная одноосновная карбоновая кислота.
Уксусная кислота представляет собой бесцветную жидкость с характерным резким запахом и кислым вкусом. Гигроскопична. Неограниченно растворима в воде. Химическая формула CH3COOH.
70-80% водный раствор уксусной кислоты называют уксусной эссенцией, а 3-6% — уксусом. Водные растворы уксусной кислоты широко используются в пищевой промышленности и бытовой кулинарии, а также в консервировании.
Продукт естественного скисания виноградных сухих вин и сбраживания спиртов и углеводов. Участвует в обмене веществ в организме. Широко применяется в приготовлении консервов, маринадов, винегретов.
Уксусную кислоту применяют для получения лекарственных и душистых веществ, как растворитель (например, в производстве ацетилцеллюлозы, ацетона). Она используется в книгопечатании и крашении.
Соли и эфиры уксусной кислоты называют ацетатами.
Пищевая добавка Е260 всем известна как уксусная кислота или уксус. Добавка Е260 используется в пищевой промышленности в качестве регулятора кислотности. В основном уксусная кислота применяется в виде водных растворов в пропорции 3-9% (уксус) и 70-80% (уксусная эссенция). Добавка Е260 имеет характерный резкий запах. В водных растворах регулятор кислотности Е260 представляет собой довольно слабую кислоту. В чистом же виде уксусная кислота представляет собой бесцветную едкую жидкость, поглощающую влагу из окружающей среды и замерзающую уже при температуре 16,5 °C с образованием твердых бесцветных кристаллов. Химическая формула уксусной кислоты: C 2 H 4 O 2 .
Уксус был известен еще несколько тысячелетий назад, как естественный продукт брожения пива или вина. В 1847 году немецкий химик Герман Кольбе впервые синтезировал уксусную кислоту в лабораторных условиях. Сейчас в мире природным методом добывается лишь 10% общего объема производства уксусной кислоты. Но натуральный метод брожения по прежнему важен, так как во многих странах действуют законы, согласно которым в пищевой промышленности должна использоваться лишь уксусная кислота биологического происхождения. При биохимическом производстве добавки Е260 используется способность некоторых бактерий окислять этанол (спирт). Данный метод известен как уксуснокислое брожение. В качестве сырья для производства добавки Е260 используются забродившие соки, вино или же раствор спирта в воде. Существует также ряд методов синтезирования уксусной кислоты в промышленности. Самый популярный из них, на который приходится более половины мирового синтеза уксусной кислоты, заключается в карбонилировании метанола в присутствии катализаторов. Исходными составляющими для данной реакции являются метанол (CH 3 OH) и окись углерода (CO).
Уксусная кислота имеет важное значение для работы человеческого организма. Ее производные помогают расщеплять в организме углеводы и жиры, поступающие в организм с продуктами питания. Уксусная кислота выделяется при жизнедеятельности некоторых видов бактерий, в частности Clostridium acetobutylicum и бактерий рода Acetobacter . Эти бактерии встречаются повсеместно в воде, почве, продуктах питания и естественным путем попадают в организм человека.
Токсическое воздействие добавки Е260 на организм человека зависит от степени разбавления уксусной кислоты водой. Опасным для здоровья и жизни считаются растворы, в которых концентрация уксусной кислоты выше 30%. Высококонцентрированная уксусная кислота при соприкосновении с кожей и слизистыми оболочками может вызывать сильные химические ожоги.
В пищевой промышленности добавка Е260 применяется для выпечки кондитерских изделий, консервирования овощей, производства майонезов и других продуктов питания.
Регулятор кислотности Е260 разрешен для использования в пищевых продуктах во всех странах, как добавка безопасная для здоровья человека.
Уксусная кислота также используется:
- в быту (удаление накипи из чайников, уход за поверхностями);
- в химической промышленности (в качестве растворителя и химреагента);
- в медицине (получение лекарственных средств);
- в других отраслях промышленности.
Пищевой консервант Е260 Уксусная кислота хорошо знаком всем людям, которые интересуются искусством гастрономии. Этот продукт представляет собой результат скисания виноградных вин в естественных условиях, при которых происходит сбраживание спирта и углеводов. Кроме того, известно, что уксусная кислота принимает непосредственное участие в процессах обмена веществ в организме человека.
Уксусной кислоте присущ резкий запах, однако в чистом виде она представляет собой совершенно бесцветную жидкость, способную поглощать влагу из окружающей среды. Замерзать данное вещество способно при температуре минус 16 градусов, в результате образуя прозрачные кристаллы.
Примечательно, что уксусом называется 3-6% раствор уксусной кислоты, в то время как при 70-80 процентном содержании получается уксусная эссенция. Растворы Е260 на основе воды широко используются не только в пищевой промышленности, но и в бытовой кулинарии. Основное применение пищевого консерванта Е260 Уксусная кислота - изготовление маринадов и консервов.
Кроме того, активно добавляется это вещество и при промышленном производстве ряда кондитерских изделий, а также майонезов и консервированных овощей. Нередко при особой необходимости пищевой консервант Е260 Уксусная кислота может быть применен в качестве дезинфицирующего и обеззараживающего средства.
Однако область изготовления продуктов питания - не единственная сфера использования пищевого консерванта Е260. Так, его широко применяют в химическом производстве при получении органического стекла, ацетатного волокна, а также при изготовлении эфиров и медикаментов.
Кстати, в фармакологии широко используют так называемый уксусный эфир, который более известен человеку под названием ацетилсалициловая кислота или аспирин. В качестве растворителя уксусная кислота тоже помогает людям в ряде случаев, а выделенные из ее состава соли успешно используются в борьбе с вредителями растений.
Вред пищевого консерванта Е260 Уксусная кислота
Вред пищевого консерванта Е260 Уксусная кислота для человека особенно очевиден при употреблении данного вещества в высоких концентрациях, так как в таком виде оно очень токсично. К слову, степень токсичности кислоты напрямую зависит от того, насколько ее разбавили водой. Самыми опасными для здоровья считаются растворы, концентрация которых превышает 30 процентов. При контакте слизистых оболочек или кожи с концентрированной уксусной кислотой возникают сильнейшие химические ожоги.
Пищевой консервант Е260 Уксусная кислота допущен для использования в пищевой промышленности во всех странах мира, так как не считается опасным для здоровья. Единственное, что рекомендуют специалисты во избежание вероятного вреда пищевого консерванта Е260 Уксусная кислота - ограничить употребление продуктов с данным веществом в составе людям с заболеваниями печени и ЖКТ. Такие продукты не советуют давать и детям младше 6-7 лет.
Уксусная кислота
Летучими кислотами вина называют входящие в его состав одноосновные кислоты жирного ряда с общей формулой.
Это муравьиная, уксусная, пропионовая, масляная, валериановая, каприловая и другие высшие жирные кислоты. Главной среди летучих кислот по своему количеству и значению является уксусная кислота . Все аналитические определения летучей кислотности вин производят в пересчете на уксусную кислоту.
Летучие кислоты вина – побочные продукты спиртового брожения. При брожении наименьшее количество летучих кислот образуется в интервале температур от 15 ºС до 25 ºС. Более высокие и более низкие температуры брожения способствуют образованию большей массы летучих кислот. При аэробных условиях брожения летучих условий образуется меньше.
Летучие кислоты перегоняются с водяным паром. Это свойство лежит в основе всех методов их количественного определения.
Соли летучих кислот легко растворимы в воде и спирте. Эфиры летучих кислот в небольших количествах являются желательной составной частью букетистых веществ вин и коньяков.
Уксусная кислота (CH3COOH) известна с давних времен. Её кислотный радикал носит название «Ацетил » от латинского обозначения кислоты – « Acidum Aceticum » . В чистом виде безводная уксусная кислота представляет собой бесцветную жидкость с острым запахом, которая затвердевает в кристаллическую массу при температуре ниже 16 ºС. Температура кипения уксусной кислоты + 118,5 ºС.
Как сама уксусная кислота, так и её соли находят применение в технике. Соли используются в текстильной, химической промышленности, в кожевенном и резиновом производстве. Сама уксусная кислота идет для приготовления ацетона, ацетатов целлюлозы, душистых веществ, применяется в медицине, пищевой промышленности, служит для приготовления маринадов.
Свинцовый уксус (CH 3 COOH )2· Pb · Pb (OH )2 Используется в производстве белил и в химическом анализе для осаждения фенольных веществ.
На основе уксусной кислоты готовят так называемый столовый уксус, который широко используется в небольших количествах для сдабривания различных блюд. Большим спросом в кулинарии пользуется натуральный винный уксус, получаемый из вина.
Для приготовления винного столового уксуса разбавленное водой вино слегка подкисляют уксусом и помещают в плоские чаны или открытые бочки. На поверхность жидкости наносят пленку уксусных бактерий. Широкий доступ воздуха (аэрация), повышенная температура и полное отсутствие сульфитации способствуют быстрому развитию уксуснокислых бактерий и быстрому превращению этилового спирта в уксусную кислоту.
Уксусная кислота – обязательный побочный продукт спиртового брожения и составляет основную долю летучих кислот.
Повышение содержания летучих кислот в винах объясняются возникновением их при многих болезнях вин и в результате деятельности различных болезнетворных бактерий. Самой опасный и в то же время наиболее часто встречающейся болезнью вин является Уксусное скисание. При этой болезни этиловый спирт род действием уксусных бактерий (Bact. aceti и др.) окисляется в уксусную кислоту:
Предупреждает возникновение в вине уксусного скисания своевременная доливка, хранение виноматериалов при температурах 10-12 ºС, умеренная сульфитация. Уксусные бактерии являются аэробами и весьма чувствительны к сернистой кислоте, ограничивающей доступ к вину кислорода.
Для исправления вин, больных уксусным скисанием, можно культивировать на поверхности вина хересной пленки. Развиваясь на вине, хересные дрожжи значительно уменьшают содержание летучих кислот. Столовые вина с повышенным (более 4 г/дм3) содержанием летучих кислот после удаления уксусной плёнки пастеризуют для умерщвления уксусных бактерий, спиртуют и употребляют в купажи ординарных крепких вин. Уничтожить уксусные бактерии можно так же сульфитацией в дозе не менее 100 мг/дм3 с немедленной обработкой бентонитом и фильтрацией вина.
Летучие кислоты вина - 3.0 out of 5 based on 3 votes
Работами Кольбе строение уксусной кислоты, а вместе с тем и всех других органических кислот было окончательно выяснено и роль последующих химиков свелась только к делению - в силу теоретических соображений и авторитета Жерара, формул Кольбе пополам и к переведению их на язык структурных воззрений, благодаря чему формула C2H6.C2O4H2 превратилась в CH3.CO(OH).
2. Свойства уксусной кислоты
Карбоновые кислоты - органические соединения, содержащие одну или несколько карбоксильных групп –СООН, связанных с углеводородным радикалом.
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризации связи О–Н. В водном растворе карбоновые кислоты диссоциируют на ионы:С увеличением молекулярной массы растворимость кислот в воде уменьшается. По числу карбоксильных групп кислоты подразделяются на одноосновные (монокарбоновые) и многоосновные (дикарбоновые, трикарбоновые и т.д.).
По характеру углеводородного радикала различают кислоты предельные, непредельные и ароматические.
Систематические названия кислот даются по названию соответствующего углеводорода с добавлением суффикса -овая и слова кислота . Часто используются также тривиальные названия.
Некоторые предельные одноосновные кислоты
|
Формула |
Название |
|
|
систематическое |
тривиальное |
|
|
метановая |
муравьиная |
|
|
этановая |
уксусная |
|
|
пропановая |
пропионовая |
|
|
бутановая |
масляная |
|
|
пентановая |
валерьяновая |
|
|
гексановая |
капроновая |
|
|
пентадекановая |
пальмитиновая |
|
|
гептадеканова |
стеариновая |
|
Карбоновые кислоты проявляют высокую реакционную способность. Они вступают в реакции с различными веществами и образуют разнообразные соединения, среди которых большое значение имеют функциональные производные , т.е. соединения, полученные в результате реакций по карбоксильной группе.
2.1 Образование солей а) при взаимодействии с металлами:
2RCOOH + Mg ® (RCOO)2Mg + H2
б) в реакциях с гидроксидами металлов:
2RCOOH + NaOH ® RCOONa + H2O
Вместо карбоновых кислот чаще используют их галогенангидриды: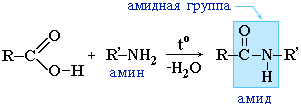 |
Амиды играют важную роль в природе. Молекулы природных пептидов и белков построены из a-аминокислот с участием амидных групп - пептидных связей.
Уксусная (этановая кислота).
Формула: СН 3 – СООН; прозрачная бесцветная жидкость с резким запахом; ниже температуры плавления (т.пл. 16,6 градусов С) похожая на лед масса (поэтому концентрированную уксусную кислоту называют также ледяной уксусной кислотой). Растворима в воде, этаноле.
Таблица 1. Физические свойства уксусной кислоты
| Название | Формула кислоты |
Раство- римость (г/100мл H2O;25°C) | Ka (при 25°С) |
|||||
|
её соли (эфиры) |
||||||||
|
уксусная |
этановая | |||||||
Похожие статьи
-
Английский - часы, время
Всем кто интересуется изучением английского языка, приходилось сталкиваться со странными обозначениями p. m. и a. m , и вообще, везде, где упоминается о времени, почему-то используется всего 12 часовой формат . Наверное, для нас живущих...
-
"Алхимия на бумаге": рецепты
Doodle Alchemy или Алхимия на бумаге на Андроид — интересная головоломка с красивой графикой и эффектами. Узнайте как играть в эту удивительную игру, а также найдите комбинации элементов для прохождения игры Алхимия на бумаге. Игра...
-
Не запускается Batman: Arkham City (Batman: Аркхем Сити)?
Если вы столкнулись с тем, что Batman: Arkham City тормозит, вылетает, Batman: Arkham City не запускается, Batman: Arkham City не устанавливается, в Batman: Arkham City не работает управление, нет звука, выскакивают ошибки, в Batman:...
-
Как отучить от игровых автоматов человека Как отучить играть в азартные игры
Вместе с психотерапевтом московской клиники Rehab Family и специалистом в терапии игромании Романом Герасимовым «Рейтинг Букмекеров» проследил путь игромана в ставках на спорт – от формирования зависимости до обращения к врачу,...
-
Ребусы Занимательные ребусы головоломки загадки
Игра "Загадки Ребусы Шарады": ответ к разделу "ЗАГАДКИ" Уровень 1 и 2 ● Не мышь, не птица - в лесу резвится, на деревьях живёт и орешки грызёт. ● Три глаза - три приказа, красный - самый опасный. Уровень 3 и 4 ● Две антенны на...
-
Сроки поступления средств на ЯД
СКОЛЬКО ИДУТ ДЕНЬГИ НА СЧЕТ КАРТЫ СБЕРБАНКА Важные параметры платежных операций – сроки и тарифы зачисления денежных средств. Эти критерии прежде всего зависят от выбранного способа перевода. Какие условия перечисления денег между счетам
